Β-Globin
In diesem Artikel werden wir die faszinierende Welt von Β-Globin und alles, was es zu bieten hat, erkunden. Von seinen Anfängen bis zu seinen Auswirkungen auf die heutige Gesellschaft und seinen Anwendungen in verschiedenen Bereichen war Β-Globin seit langem Gegenstand von Interesse und Forschung. Auf den folgenden Seiten werden wir alle Aspekte im Zusammenhang mit Β-Globin gründlich analysieren und eine vollständige und detaillierte Vision liefern, die es uns ermöglicht, seine Bedeutung und seinen Einfluss auf unser tägliches Leben besser zu verstehen. Begleiten Sie uns auf dieser Tour durch Β-Globin und entdecken Sie alles, was dieses Thema zu bieten hat.
| β-Globin | ||
|---|---|---|
| ||
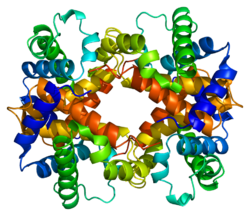
| Struktur von β-Globin im Homotetramer | ||
| Bezeichner | ||
| Gen-Name(n) | HBB, CD113t-C, beta-globin | |
β-Globin, beta-Globin, oder Hämoglobin beta-Kette ist ein Protein aus der Familie der Globine, dessen 147 Aminosäuren lange Polypeptidkette ein Häm als Cofaktor bindet und das so als Hämoglobin-Untereinheit beta (HBB) Teil von Hämoglobin-Proteinkomplexen in Wirbeltieren ist.[1] Beim erwachsenen Menschen wird für den Sauerstofftransport als häufigste Form des Hämoglobins ein Tetramer aus zwei beta- und zwei alpha-Ketten (HBA) gebildet, das sogenannte adulte Hämoglobin A (HbA(1) – α2β2).
Genort
Beim Menschen wird β-Globin (HBB) vom HBB-Gen codiert, das im Gen-Cluster des β-Globin-Locus (5′ - HBE1 – HBG2 – HBG1 – HBD – HBB -3′)[2] auf Chromosom 11 liegt. Die Expression dieser einander sehr ähnlichen Gene wird hier über eine gemeinsame Locus-Kontrollregion (LCR)[3] gesteuert und ist entwicklungsabhängig verschieden. Je nach Entwicklungsphase bzw. Zellmilieu kann die Proteinbiosynthese von entsprechenden ε-, γ-, δ- oder β-Globinen veranlasst werden.[4]
Die gebildeten Proteine unterscheiden sich voneinander nur in wenigen Aminosäuren ihrer jeweils 147 AS langen Kette; doch zeigen die aus ihnen zusammengesetzten Hämoglobine Unterschiede im Sauerstoff-Bindungsvermögen. Während vorgeburtlich epsilon- (für embryonales Hämoglobin) und gamma-Globin (für fetales Hämoglobin, HbF) gebildet werden, sind es nach der Geburt normalerweise überwiegend beta- und seltener delta-Globin (für adultes Hämoglobin, HbA(1) – α2β2 bzw. HbA2 – α2δ2).
Erkrankungen
Mutationen im Gen für β-Globin sind Ursache einer Erkrankung von roten Blutkörperchen, bei der typische Veränderungen ihrer Form auftreten, der Sichelzellenanämie. Das Fehlen von beta-Ketten verursacht eine Thalassemia major (auch ß0-Thalassämie); bei der Thalassemia minor (auch ß+-Thalassämie) ist die Menge von nachweisbarem β-Globin vermindert, die Symptome sind wenig ausgeprägt.[1]
Interaktionen
HBB weist mit dem α-Globin Protein-Protein-Interaktion auf.[5][6]
Einzelnachweise
- ↑ a b Entrez Gene: HBB hemoglobin, beta. Abgerufen am 11. Mai 2012.
- ↑ Entrez Gene: HBE1 hemoglobin, epsilon 1. Abgerufen am 19. Mai 2012.
- ↑ Levings PP, Bungert J: The human beta-globin locus control region. In: Eur. J. Biochem. 269. Jahrgang, Nr. 6, März 2002, S. 1589–99, doi:10.1046/j.1432-1327.2002.02797.x, PMID 11895428.
- ↑ Higgs DR, Vickers MA, Wilkie AO, Pretorius IM, Jarman AP, Weatherall DJ: A review of the molecular genetics of the human alpha-globin gene cluster. In: Blood. 73. Jahrgang, Nr. 5, Mai 1989, S. 1081–104, PMID 2649166.
- ↑ Ulrich Stelzl, Worm Uwe, Lalowski Maciej, Haenig Christian, Brembeck Felix H, Goehler Heike, Stroedicke Martin, Zenkner Martina, Schoenherr Anke, Koeppen Susanne, Timm Jan, Mintzlaff Sascha, Abraham Claudia, Bock Nicole, Kietzmann Silvia, Goedde Astrid, Toksöz Engin, Droege Anja, Krobitsch Sylvia, Korn Bernhard, Birchmeier Walter, Lehrach Hans, Wanker Erich E: A human protein-protein interaction network: a resource for annotating the proteome. In: Cell. 122. Jahrgang, Nr. 6. United States September 2005, S. 957–68, doi:10.1016/j.cell.2005.08.029, PMID 16169070 (englisch).
- ↑ B Shaanan: Structure of human oxyhaemoglobin at 2.1 A resolution. In: J. Mol. Biol. 171. Jahrgang, Nr. 1. England November 1983, S. 31–59, doi:10.1016/S0022-2836(83)80313-1, PMID 6644819 (englisch).
Literatur
- Higgs DR, Vickers MA, Wilkie AO, et al.: A review of the molecular genetics of the human alpha-globin gene cluster. In: Blood. 73. Jahrgang, Nr. 5, 1989, S. 1081–104, PMID 2649166.
- Giardina B, Messana I, Scatena R, Castagnola M: The multiple functions of hemoglobin. In: Crit. Rev. Biochem. Mol. Biol. 30. Jahrgang, Nr. 3, 1995, S. 165–96, doi:10.3109/10409239509085142, PMID 7555018.
- Salzano AM, Carbone V, Pagano L, et al.: Hb Vila Real in Italy: characterization of the amino acid substitution and the DNA mutation. In: Hemoglobin. 26. Jahrgang, Nr. 1, 2002, S. 21–31, doi:10.1081/HEM-120002937, PMID 11939509.
- Frischknecht H, Dutly F: A 65 bp duplication/insertion in exon II of the beta globin gene causing beta0-thalassemia. In: Haematologica. 92. Jahrgang, Nr. 3, 2007, S. 423–4, doi:10.3324/haematol.10785, PMID 17339197.