Natriumperiodat
Heutzutage ist Natriumperiodat für eine Vielzahl von Menschen zu einem Thema von großem Interesse geworden. Von Experten auf diesem Gebiet bis hin zu Informationssuchenden zu diesem Thema stellt Natriumperiodat für viele einen interessanten Punkt dar. Ob aufgrund seiner historischen Bedeutung, seiner Auswirkungen auf die heutige Gesellschaft oder seiner Relevanz im wissenschaftlichen Bereich – Natriumperiodat ist nach wie vor ein Thema, das große Debatten und Faszination hervorruft. In diesem Artikel werden wir die verschiedenen Facetten von Natriumperiodat und seine Relevanz in der heutigen Welt untersuchen und einen vollständigen und aktuellen Überblick über das Thema geben.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
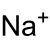 
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Natriumperiodat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | NaIO4 | |||||||||||||||
| Kurzbeschreibung |
farb- und geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 213,89 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
3,87 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
mäßig in Wasser (91 g·l−1 bei 20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Natriumperiodat ist eine chemische Verbindung aus der Gruppe der Periodate (genauer das Natriumsalz der Metaperiodsäure). Es liegt in Form eines sehr reaktionsfähigen, brandfördernden, geruch- und farblosen Pulvers vor.
Vorkommen
Natriumperiodat kommt natürlich in geringen Mengen als Beimengung von Chilesalpeter vor.
Gewinnung und Darstellung
Natriumperiodat kann aus Natriumiodat dargestellt werden.[2]
Eigenschaften
Bei Erhitzung über 300 °C zersetzt sich Natriumperiodat, wobei Natriumoxid und Iod (oder bei Anwesenheit von Feuchtigkeit Iodwasserstoff) entstehen. Natriumperiodat kristallisiert tetragonal, Raumgruppe I41/a (Raumgruppen-Nr. 88), mit den Gitterparametern a = 5,337 Å und c = 11,95 Å.[3]
Verwendung
Natriumperiodat wird als Maßlösung eingesetzt. Es kann auch zur Herstellung von 1-Pyrrolin und als Oxidationsmittel (z. B. bei Dihydroxylierungen als Cooxidans) verwendet werden. In der Bioorganischen Chemie dient es zur selektiven Oxidation von aminoterminalen Serinen in Peptiden oder Proteinen. Auf diese Weise werden Glyoxalfunktionen erzeugt. Diese aldehydischen Gruppen können mit primären Aminen in Schiff'sche Base Reaktionen zur Biokonjugation verwendet werden. Aldehydfunktionen können auch mittels Natriumperiodat vermittelter Oxidation aus 1,2-Diolen, welche in Zuckerresten glycosilierter Biomoleküle vorkommen, erzeugt werden.
Sicherheitshinweise
Natriumperiodat selbst brennt nicht, aber es kann bestehende Brände erheblich fördern und reagiert heftig mit brennbaren Stoffen, so dass es bei Kontakt mit solchen zu einer Selbstentzündung kommen kann.
Einzelnachweise
- ↑ a b c d e f Eintrag zu Natriumperiodat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6.
- ↑ A. Kalman, D.W.J. Cruickshank: Refinement of the Structure of NaIO4. In: Acta Crystallographica, B26, 1970, S. 1782–1785, doi:10.1107/S0567740870004880.





